اللوپاتی گندم
علف
های هرز جزء محدود کنندهای اصلی عملکرد محصولات زراعی در اکثر سیستم های
کشاورزی و بخصوص سیستم ارگانیک هستند. در سیستم کشاورزی مرسوم، علف های هرز
توسط علفکش ها کنترل می شوند اما این فعالیت نگرانی هایی را در مورد سلامت
انسان و محیط در پی داشته است. استفاده گسترده از علفکش ها یک مشکل جدید
به نام علف های هرز مقاوم به علفکش به وجود آورده است(2).
اثرات
آللوپاتی، ناشی از مواد بازدارنده ای است که بصورت مستقیم توسط گیاهان زنده
به محیط وارد شده اند یا شامل تمامی ترشحات ریشه، مواد حاصل از آبشویی،
تبخیر و بقایای گیاهی تجزیه شده، می باشد. Whittaker و Feeuy مواد سمی
گیاهی را آللوکمیکال نامیدند. استفاده از آللوپاتی برای کنترل علف های هرز
مطالعات زیادی را در چند دهه گذشته بخود اختصاص داده است(7).
گندم
یکی از غذاهای اصلی در جهان است که آزمایشات بین المللی زیادی برای ارزیابی
توانایی آللوپاتیک آن در جلوگیری از رشد علف هرز در جهان صورت گرفته است.
اولین بررسی ها در اواخر دهه 1960 نشان داد که آللوپاتی بقایای گندم در بین
ارقام متفاوت است(6). گیاهچه ها، کاه وکلش و عصاره آبی بقایای گندم باعث
بروز اثرات آللوپاتی بروی رشد تعدادی از علف های هرز می شود. آللوپاتی گندم
معمولا با کاهش شیوع آفات و بیماریها همراه است.
تحقیقات بر روی
آللوپاتی گندم به بررسی اثر آللوپاتی گندم بر دیگر گیاهان زراعی، علف های
هرز، آفات و بیماریها، همچنین استخراج و خالص سازی و تشخیص عوامل
آللوپاتیک، خودمسمومی گندم، و مدیریت بقایای گندم می پردازد انتخاب واریته
های مختلف گندم برای ارزیابی میزان پتانسیل آللوپاتیکشان در توقف علف های
هرز و مطالعه بر رفتارهای ژنتیکی برای صفات آللو پاتیک، در دست بررسی
است(7).
اثرات مفید آللوپاتی گندم
1. آللوپاتی گیاهچه گندم برای توقف رشد علف هرز:
آللوپاتی
گیاهچه گندم بروی علف های هرز مشخصی ارزیابی شده است. ترشحات ریشه گیاهچه
های گندم حاوی 5 Benzoxazinones و 7 فنولیک اسید می باشد. بالاترین غلظت
ترکیبات آللوکمیکال در هر دو گروه شیمیایی در 8 روز پس از جوانه زنی اتفاق
افتاد که این به خوبی با حداکثربازدارندگی رشد چچم توسط ترشحات ریشه گندم
در این دوره مشاهده شد. که این مطلب حاکی از آن است که مواد شیمیایی قوی
آللوپاتیک بازدارنده، در ترشحات ریشه وجود دارد(6).
Spruell در سال
1984، 284 توده گندم را برای ارزیابی پتانسیل آللوپاتیکشان در ایالات متحده
غربال کرد. ترشحات ریشه هر توده با سویه T64، برای بازدارندگی رشد ریشه و
ساقه در بروموس و سلمه مقایسه شد. 5 توده ترشحات ریشه ای تولید کردند که به
طور معنی داری نسبت به سویه T64 اثرات بازدارندگی روی رشد ریشه های علف
هرز داشتند.
Hashem و Adkins در سال 1998 غربال ارقام مختلف گندم را
برای تعیین آللوپاتی گیاهچه بر رشد یولاف وحشی و خاکشیر آزمایش کردند و
دریافتند که از 17 توده، T. speltoids بازدارنده رشد طولی ریشه یولاف وحشی
است و 2 تا از 19 توده بازدارنده رشد طولی ریشه چه در خاکشیر می باشد (7).
در
سال 2000 Wu و همکاران، توانایی آللوپاتی 453 توده گندم از 50 کشور را بر
رشد چچم یکساله بررسی کردند و تفاوت معنی داری از نظر بازدارندگی رشد ریشه
چچم از 9/90 – 7/9 درصد گزارش دادند. توانایی آللوپاتی گیاهچه گندم از
کشورهای مختلف،تفاوت معنی داری نشان می دهد که این نشان دهنده دخالت چند ژن
برای بیان صفت آللوپاتی است. از 453 توده، 63 توده اثرات آللوپاتیک بسیار
قوی داشتند که اثر بازدارندگی آنها بیش از 81 درصد روی رشد ریشه چچم بود،
در حالیکه 21 توده اثر آللوپاتیکی ضعیفی داشتند و اثر بازدارندگی آنها کمتر
از 45 درصد بروی چچم بود.
میزان آللوپاتی گیاهچه گندم بطور معنی
داری با کشور مبدا مرتبط است. توده هایی افغانستان، کانادا، لهستان دارای
اثرات آللوپاتیک ضعیفی بودند در حالیکه توده هایی از آلمان، مکزیک و
آفریقای جنوبی اثر آللوپاتیکی بسیار قوی داشتند(9).
در آزمایشهای
انجام شده توسط ریزوی و همکاران در سال 2000 توده های گندم، یک تفاوت
ژنتیکی معنی دار بین 10+ تا 30- درصد نشان دادند. ارقامی مانند قدس، خزر1،
4512PI به ترتیب موجب 9/27، 3/28 و 2/30 درصد کاهش در وزن خشک علف هرز
(یولاف) شدند. ارقام bezostaya-1 ، نوید و نوید نژاد آللوپاتی مثبت داشتند و
وزن خشک یولاف را به ترتیب 6/6، 9/10 و 4/10 درصد افزایش دادند. افزایش در
تراکم بذر گندم بازدارندگی آللوپاتی یولاف را تقویت نمود اما باعث هیچ
گونه خودمسمومی نشد. این نتایج نشان می دهد که بعضی از توده های گندم حامل
ژن هایی برای صفات آللوپاتی (هم افزایش هم بازدارندگی) هستند که می تواند
برای اصلاح ارقام گندم دارای توانایی آللوپاتی به منظور کنترل علف های هرز
مورد استفاده قرار گیرد(5).
در آزمایش سه ساله ای که ریزوی و
همکاران انجام دادند، بیش از 200 توده گندم مورد ارزیابی قرار گرفت که پس
از غربال، 29 توده امیدبخش انتخاب شدند و برای کنترل علف های هرز در شرایط
مزرعه و گلخانه مورد بررسی قرار گرفتند که دو رقم، باعث 62 و 75 درصد کاهش
رشد علف هرز شدند.بنابراین، ارقامی از گندم وجود دارند که می توانند جمعیت
علف هرز را به زیر سطح آستانه بیاورند (4).
در سال 2000 Wu و
همکاران، توانایی آللوپاتی 92 توده گندم را از نظر بازدارندگی رشد ریشه چچم
یکساله بررسی کردند. توانایی آللوپاتی گندم، به زمان کاشت بذر چچم و تعداد
گیاهچه گندم بستگی داشت. بین ارقام گندم در مرحله گیاهچه ای از نظر
توانایی آللوپاتی بر رشد طولی ریشه چچم یکساله، تفاوت معنی داری بین 91/90 –
98/23 درصد وجود داشت. تداخل بین گیاه زراعی و علف هرز در اوایل مرحله
جوانه زنی، بحرانی است و اگر یک گونه علف هرز را بتوان با استفاده از
آللوپاتی گیاهان زراعی در طی دوره استقرار بازداشت، گیاه زراعی بعدا برتری
بیشتری نسبت به علف های هرز خواهد یافت(10).
2. آللوپاتی بقایای گندم برای توقف رشد علف هرز:
گندم
به صورت موفقیت آمیزی همچون یک گیاه پوششی برای کنترل علف هرز در سیستم
های مختلف کشت مورد استفاده قرار می گیرد. گیاهان پوششی مثل گندم، چاودار،
سورگوم یا جو تا ارتفاع 40 تا 50 سانتیمتر رشد می کنند و سپس با یک علف کش
تماسی خشک می شوند.Putnam و همکارانش در سال 1983 گزارش دادند که باقی
گذاشتن بقایای گیاهان زراعی در سطح خاک باعث کنترل بیش از 95 درصد علف های
هرز در مدت 30 تا 60 روز پس از خشک شدن گیاهان پوششی می شود. در بین 9 گیاه
زراعی پوششی چچم پر گل (Italian ryegrass)، چچم پایدار
(perennialryegrass)،علف بره قرمز (Festuca rubra L. spp.) Commutata،علف
بره نی مانند (Festuca arundinacea Schreb)، شبدر سفید، چچم، گندم، جو و
یولاف، گندم با کنترل شیمیایی ساده، موجب جلوگیری از رشد علف های هرز می
شود، و اثرات بازدارندگی بسیار کمی بر روی جوانه های ایجاد شده خیار، سویا،
لوبیا، نخود و ذرت دارد(7).
آزمایشات نشان می دهد که عصاره آبی
بقایای گندم بروی تعدادی از علف های هرز اثر آللوپاتیک دارد و باعث کاهش
جوانه زنی و رشد علف های هرز می شود. در شرایط آزمایشگاهی، عصاره استخراج
شده از کاه و کلش گندم اثرات آللوپاتیک را بروی طیف وسیعی از گونه های علف
هرز نشان داد.
Steinsiek و همکارانش در سالهای 1980 و 1982 گزارش
کردند که گونه های علف هرز پاسخهای متفاوتی به عصاره آبی از خود نشان می
دهند، درIpomoea hederacea L. و گاو پنبه بیشترین بازدارندگی و سوروف،
Ipomoea lacunose L. و Cassia obtusifolia L. کمترین اثر بازدارندگی دیده
شده است. این نتایج نشان می دهد که آللوکمیکال های موجود در کاه و کلش
گندم، در خاک تحت اثر شستشو و باعث بروز اثرات انتخابی روی رشد علف های هرز
مشخص در مجاورت خود شود(7).
آللوپاتی بقایای گندم در بین واریته ها
متفاوت است. در استرالیا، 38 توده گندم برای ارزیابی توانایی آللوپاتی
بقایا بروی چچم یکساله توسط عصاره استخراج شده از کلش مورد بررسی قرار
گرفتند. نتایج نشان داد که جوانه زنی و رشد ریشه چچم یکساله بطور معنی داری
توسط عصاره آبی استخراج شده از بقایای گندم کاهش می یابد و بین توده های
گندم اثر بازدارندگی بطور معنی داری متفاوت است.میزان بازدارندگی رشد ریشه
در حدود 19.2درصد تا 98.7 درصد و برای جوانه زنی بذرها از 4.2 درصد تا 73.2
درصد متغییر می باشد. برای آزمایش توده های مختلف گندم برضد گونه های
مقاوم چچم یکساله به علف کشهای (گروه A) بازدارنده های استیل COA
کربوکسیلاز، (گروه B) بازدارنده های استولاکتات سنتتاز، (گروه C) بازدارنده
های فتوسیستم 2 و (گروهD ) بازدارندهای تشکیل توبولین (tubulin)، بکار
رفتند. نتایج نشان داد که عصاره آبی گندم بطور معنی داری باعث بازدارندگی
جوانه زنی و رشد ریشه این گونه های زیستی مقاوم، می شود، میزان بازدارندگی
جوانه زنی از 3.3 درصد تا 100 درصد بود که میزان آن بسته به توده ها متغیر
بود. در مقایسه با شاهد میزان تغییر رشد ریشه در اثر مواد آللوپاتیک روی
چچم از 12 دزصد تحریک کنندگی تا 100 درصد بازدارندگی متغیر بود. این نتایج
نشان میدهد که آللوپاتی گندم می تواند توانایی کنترل گونه های مختلف مقاوم
به علف کش ها را داشته باشد (8).
Murray و Thilsted دریافتند که
بازدارندگی تاج خروس در کرتهای پوشیده با کاه و کلش گندم بطور تقریبی با
نتایج حاصل از کرتهای بدون مالچ با مصرف علف کش مشابه است. Banks و
robinsonهمچنین گزارش دادند که مالچ کاه و کلش گندم باعث توقف رشد علف های
هرز Amaranthus spinosus L. و Ipomoea purpurea L. می شود، و وجود گندم در
زمینهای بدون پوشش بیش از مصرف علف کش ها موثر است. Shilling و همکارانش
نشان دادند که مالچ گندم دارای اثرات بازدارنده آللوپاتیک بر برخی علف های
هرز پهن برگ می باشد. آللوکمیکال های موجود در بقایای گندم در سیستم های
بدون شخم بعنوان مالچ باقیمانده می تواند علف های هرز را در گیاه زراعی
بعدی کنترل کند. همچنین استفاده از کاه و کلش گندم برای توقف علف هرز در
جنگل زراعی ها هم گسترش یافته است. Jobidon نشان داد که عصاره آبی کاه و
کلش گندم از رشد علف هرز معمول جنگل به نام Rubus idaeus L. تا 44 درصد جلو
گیری می کند. این اثرات آللو پاتیک مجددا در مزرعه تائید شد (7).
Guenzi
و همکاران دریافتند که بقایای گندم بعد از گذشت 8 هفته در شرایط مزرعه
دیگر حاوی ترکیبات سمی محلول در آب نیستند. بنابراین مواد سمی می توانند،
مخصوصا در خاکهای با زهکش ضعیف توسط باران از بقایای کاه و کلش گندم به
درون خاک، آبشویی شوند.
Banks و Robinson همچنین نشان دادند که مالچ
کاه و کلش از رشد تاج خروس و Ipomoea purpurea L. جلوگیری می کند و گندم
ناخواسته نسبت به علف کشهای استفاده شده در مناطق بدون مالچ باعث بروز
اثرات موثرتری می شود.
Guenzi
و همکاران نشان دادند که مواد سمی عصاره آبی کاه و کلش 9 واریته گندم در
اثر بازدارندگی بروی جوانه زنی و رشد گیاهچه گندم متفاوت بودند (3).
گندم
خشک شده با علف کش گلیفوزیت و پاراکوات، زیتوده علف های هرز را 88- 76
درصد کاهش می دهد. مالچ گندم مسئول کاهش جمعیت نیلوفر (Ipomea lacunose) و
علف های هرز دیگر در سیستم بدون شخم گندم است. وجود فرولیک اسید و ترکیبات
دیگری را مسئول کاهش رشد علف های هرز در سیستم بدون شخم، می دانند.
سمیت
بقایای گندم در مراحل معینی از رشد بیشتر است و با گذشت زمان، کاهش می
یابد. بطور کلی، هر چه زمان تجزیه بقایای گیاه زراعی طولانی تر باشند، از
انباشتگی مواد سمی در خاک کاسته می شود. کاه و کلش گندم، جمعیت علف های هرز
پهن برگ را 16.8 درصد کاهش می دهد، اما اثری بر علف های هرز باریک برگ
ندارد. البته کاه و کلش گندم، زیتوده هر دو نوع علف هرز را کاهش می دهد.
افت زیتوده تا 120 روز پس از بذر افشانی افزایش اما پس از آن، کاهش می
یابد. توانائی دگر آسیبی بقایای گندم تحت تاثیر سن، مقدار آب، کربن،
نیتروژن و pH خاک تعیین می گردد.
عصاره های آبی بقایای گندم با غلظت
2 و 4 درصد از جوانه زنی بذر، رشد ریشه، نوشاخه و گیاه کامل، می کاهد. اثر
بازدارندگی بر علف های هرزی نظیر تاج خروس، آشکارتر از سوروف بود. سمیت
بقایای گندم بر سوروف تا 6 هفته پایدار است و پس از آن از بین می رود(1).
اثرات زیان آور آللوپاتی گندم
1. خودمسمومی گندم:
خودمسمومی
گندم، رشد کند گیاهچه های استقرار یافته و به دنبال آن کاهش عملکرد دانه
ای گندم معمولا هنگامی رخ می دهد که قبلا کاه و کلش گندم در زمین رها شده
باشد. Alam در سال 1990 گزارش کرد که جوانه زنی و رشد گندم تحت تیمار عصاره
آبی کاه وکلش همان گونه گندم بطور معنی داری کاهش می یابد. تحقیقات نشان
می دهد که تنوع خود مسمومی گندم بسته به واریته آنهاست. بطور مثال رقم
Gaboاثر بازدارندگی قویتری نسبت به رقم Insignia نشان می دهد. مواد استخراج
شده از کاه و کلش رقم Gabo و رقم Insigniaدارای اثرات بازداندگی بر رشد
ریشه و گیاهچه گندم به میزان 27 و 4 درصد و همچنین بازدارندگی بر رشد ساقه
به میزان 43 و 12 درصد می باشند. مواد آللوپاتیک حاصل از گیاه زنده گندم و
کاه کلش گندم می تواند در زمانی که گندم بطور متوالی کشت شود، تجمع پیدا
کند.
وارد کردن گندم در یک سیستم کشت، چه بصورت تک کشتی و چه بصورت
تناوب با دیگر غلات، در مقایسه با دیگر سیستمهای کشت باعث افزایش اثرات
خودمسموی می شود، که این خود دلالت بر تجمع فیتوتوکسین ها دارد(7).
2. آللوپاتی گندم و رشد دیگر گیاهان زراعی:
Hozumi
و همکارانش در سال 1974 اظهار داشتند که عصاره آبی بقایای گندم از رشد
برنج، جو و چاودار جلوگیری می کند. بقایای گندم همچنین اثر آللوپاتیک بروی
رشد سویا دارد.narwal و همکارانش در سال 1997 گزارش دادند که عصاره های آبی
کاه و کلش گندم به طور زیان آوری روی جوانه زنی و رشد گیاهچه چندین گیاه
علوفه ای همچون ذرت، سورگوم،Pennisetum glaucum L.، Cyamopsis
tetragonolobaو Vigra unguiculata اثر می گذارد.
اثرات منفی
آللوپاتی بقایای گندم بروی رشد دیگر گیاهان زراعی همراه با رقم گندم تغییر
می کند. در آزمایشات گلخانه ای، 20 واریته گندم اثرات آللوپاتیک متفاوتی را
بروی رشد رقم Dare سویا نشان دادند البته در این آزمایش ارقام سویا در
خاکی حاوی 2 درصد از بقایایای کاه و کلش گندم رشد یافته بودند.
حساسیت
ها به آللوپاتی بقایای گندم در گیاهان زراعی متفاوت است. Putnam و همکاران
در سال 1983 گزارش دادند رشد بادمجان، ذرت، خیار، کاهو، نخود،Snapbean به
بقایای گندم واکنش های متفاوتی می دهند.Dias در سال 1991 دریافت که گندم،
یولاف و Trifolium subterraneum در واکنش به تجزیه شدن کاه و کلش گندم
متفاوت هستند.
واریته های گیاهان زراعی مختلف همچنین به آللوپاتی
بقایای گندم به طور متفاوتی واکنش نشان می دهند. Hicks و همکاران در سال
1989، 11 واریته پنبه را برای ارزیابی توانایی مقاومت به اثرات بازدارندگی
کاه و کلش گندم در آزمون زیست سنجی آزمایشگاهی و مطالعات گلخانه ای غربال
کردند.واریته مقاوم paymaster404 و واریته حساس Acala A246 برای آزمایشات
مزرعه ای انتخاب شدند. جوانه زنی پنبه به طور میانگین 9 درصد برای
Paymaster404 و 21 درصد برای Acala A246 کاهش یافت. همچنین در آزمایشات
مزرعه ای و گلخانه ای واریته های سویا به طور معنی داری در مقاومت به اثرات
آللوپاتیک بقایای گندم متفاوت بودند. واریته های Davis و Centennial
بیشترین مقاومت و Correst کمترین مقاومت را داشت.(7)
مدیریت اثرات زیان آور بقایای گندم
اثرات
زیان آور بقایای گندم توسط چند فاکتور زنده و غیر زنده تعیین می شود که
شامل ژنوتیپ، کاه و کلش، مقدار و مدت زمان تجزیه شدن، نوع خاک، نحوه کشت و
کار، خاک و شرایط اقلیمی می باشد. تحقیقات نشان می دهد که این اثرات مضر بر
محصولات کشاورزی را می توان با روشهای مدیریت موثر بر بقایای گندم کاهش
داد. تناوب دقیق و صحیح گیاهان زراعی باعث افزایش اثرات مفید آللوپاتی
همراه با کاهش میزان تجمع مواد آللوشیمیایی، می شود.
تناوب با گونه
های زراعی متحمل یا واریته های متحمل در گونه های زراعی، اثرات آللوپاتیک
کاه و کلش گندم را به حداقل می رساند. انتخاب واریته های گندم که خاصیت
آللوپاتی ندارند یا واریته هایی که متحمل به آللوپاتی هستند بعنوان گیاه
زراعی بعدی یک روش تناوب مناسب است. اگر یک واریته خاص گندم دارای خاصیت
آللوپاتیک طبیعی است، می توان یک واریته گندم متحمل به آللوپاتی را در
تناوب انتخاب نمود.
اگر انتخاب واریته های متحمل گندم امکانپذیر
نبود و مجبور بودیم کاه کلش را در زمین باقی بگذاریم، ابتدا یک واریته
گندم، با کمترین مقدار فعالیت آللوپاتیک را کشت می کنیم تا مشکلات
فیتوتوکسیک برای گیاه بعدی کاهش یابد.
ارتباط متقابل بین مقدار کاه و
کلش با خاصیت آللوپاتیکی به خوبی به اثبات رسیده است. با عواملی مثل کاهش
مقدار کاه و کلش باقیمانده، کشت زودتر، و کشت واریته های متحمل به آللوپاتی
می توان بر اثرات منفی کاه و کلش گندم غلبه کرد. میزان تجزیه اولیه بقایا
می تواند در واکنش گیاه بعدی اثر بگذارد. آللوکمیکال هایی که از بقایا شسته
شده، و وارد خاک می شوند می تواند تحت تاثیر جذب سطحی خاک، آبشویی،
تغییرات میکروبی یا پروسه های تجزیه قرار گرفته و در نتیجه خاصیت آللوپاتیک
طبیعی خود را از دست بدهند. بررسی ها نشان می دهد که بعد از مدتی که بقایا
تجزیه شدند، خاصیت آللوپاتیک از بین می رود.
تیمار کردن بذور
گیاهان زراعی قبل از کاشت با آللوکمیکال ها می تواند به منظور افزایش
مقاومت بذور به آللوپاتی گندم صورت گیرد.Cowsik و Jayachaandra گزارش کردند
که می توان با خیساندن 4 ساعته بذور گندم در اسید کافئیک (1ppm)، اسید
فرولیک (5ppm) و اسید وانیلیک (1ppm) در آنها ایجاد مقاومت کرد(7).
آللوپاتی
گندم، توانایی برای مدیریت علف های هرز، آفات و بیماریها می باشد. هم
آللوپاتی بقایای گندم و هم آللوپاتی گیاهچه گندم می تواند برای مدیریت علف
های هرز به کار رود. واریته های گندم در توانایی آللوپاتی بر ضد علف های
هرز متفاوت هستند، و انتخاب واریته هایی با توانایی آللوپاتی می تواند
بعنوان یک استراتژی مفید در مدیریت تلفیقی علف هرز استفاده شود. خودمسمومی
گندم بروی سیستم های تولید کشاورزی اثرات منفی دارد مخصوصا زمانیکه کاه
وکلش گندم بروی سطح خاک، برای اهداف کشاورزی حفاظت شده ، رها شده است. در
آینده آللوپاتی گندم نیازمند بررسی هایی در جهت افزایش توانایی آللوپاتی
برای کنتزل علف هرز، آفات و بیماری و به حداقل رساندن اثرات منفی روی گندم و
دیگر گیاهان زراعی، است.

 به ترکیبات آلی و در نهایت
به ترکیبات آلی و در نهایت 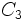 ،
، 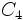 ، چرخه احیای کربن در گیاهان CAM(کراسولاسه) ، سنتز نشاسته و ساکارز در گیاهان و ... .
، چرخه احیای کربن در گیاهان CAM(کراسولاسه) ، سنتز نشاسته و ساکارز در گیاهان و ... . 
 این وبلاگ برای تمام دوستداران علوم مهندسی کشاورزی و بالاخص مهندسی مکانیزاسیون ماشین های کشاورزی و مديريت تهیه شده است . شاید قطره حتی ناچیز در راه اعتلای مکانیزاسیون کشاورزی و مديريت باشد.
این وبلاگ برای تمام دوستداران علوم مهندسی کشاورزی و بالاخص مهندسی مکانیزاسیون ماشین های کشاورزی و مديريت تهیه شده است . شاید قطره حتی ناچیز در راه اعتلای مکانیزاسیون کشاورزی و مديريت باشد.